Metode de izolare şi obţinere a culturilor pure
- Detalii
- Categorie: Merceologia mărfurilor alimentare
- Accesări: 13,222
Cultura pură reprezintă o biomasă de celule rezultate prin reproducere dintr-o singură celulă aflată într-un mediu nutritiv steril, cu volum limitat. Cultura pură este considerată şi colonia care se formează ca rezultat al izolării unei celule sau a unei unităţi formatoare de colonii, atunci când aceasta este localizată pe un mediu nutritiv solid. Puritatea unei culturi se poate obţine şi prin repicare, deci prin transfer de celule din eprubeta ce conţine cultura pură, în alt vas cu mediu de cultură steril.
În practica de laborator se cunosc numeroase metode prin care se poate realiza separarea unei singure celule din microbiota eterogenă a mediilor naturale. Metodele cunoscute şi practicate în laborator în scopul izolării culturilor pure pot fi clasificate în metode fizico-mecanice şi metode biologice.
Metode fizice de izolare şi obţinere a culturilor pure
Metode prin răspândire – se folosesc pe scară largă, fiind uşor de executat, având ca principiu răspândirea celulelor din medii naturale unde acestea se află în număr mare, prin diluare în medii lichide sau prin diseminare mecanică pe suprafaţa mediilor sterile.
Metode scarificate. În placa Petri se repartizează un mediu de cultură adecvat, de exemplu MMA/BCA şi după solidificarea mediului, cu firul metalic se recoltează celule din mediul natural şi se execută trasări pe suprafaţa mediului, astfel încât diversele celule rămân distanţate între ele. Prin termostatare 48-72 ore, din colonia care corespunde microorganismului ce trebuie izolat, se face repicare într-o eprubetă cu mediu solid înclinat şi astfel se obţine o cultură pură.
Metoda în strii este similară, în schimb drept suprafaţă de răspândire se foloseşte mediul înclinat din 2-3 eprubete, prin transferul de celule din mediul natural, prin realizarea de striuri, în mod succesiv. Aceste metode se folosesc şi în cazul în care o cultură pură este contaminată cu microorganisme străine în perioada de păstrare a culturii şi aceasta trebuie să fie salvată.
Metoda culturală Koch este folosită în special pentru izolarea de drojdii. Ca mediu de răspândire se foloseşte MMA repartizat în 3 eprubete, fluidificat şi menţinut la 40°C. Din mediul natural, de exemplu un must în fermentaţie, se recoltează o ansă care se introduce succesiv în cele 3 eprubete, cu agitare, care să asigure desprinderea celulelor. După inoculare şi uniformizare, conţinutul fiecărei eprubete se repartizează în câte o placă Petri prin solidificare celulele rămân fixate în gel şi prin multiplicare vor forma colonii izolate. În funcţie de densitatea celulelor recoltate iniţial în placa a 2-a sau a 3-a coloniile sunt suficient de distanţate (se preferă o distanţă de circa 2 cm), pentru a putea face izolarea din colonia adecvată a culturii pure, prin repicare în eprubetă cu MMA.
Metode prin diluare. În prima etapă, din mediul natural se execută diluţii decimale în ser fiziologic steril, astfel încât numărul de celule într-o micropicătură din ultima diluţie să fie redus.
Metoda Lindner se foloseşte pentru izolarea de drojdii fermentative. Din diluţia convenabilă, cu ajutorul unei peniţe topografice se plasează aprox. 9 picături pe suprafaţa unei lamele sterile. Lamela se amplasează cu picăturile în jos pe o lamă cu excavaţie şi se studiază la microscop fiecare picătură. Se notează cu un marker conturul picăturii în care se află o singură celulă. Se desprinde lamela şi cu ajutorul unei benzi sterile de hârtie se absoarbe picătura notată. Odată cu lichidul se adsoarbe şi celula de izolat, apoi banda se introduce într-o eprubetă cu mult lichid. Celula va da prin reproducere o cultură pură. Deşi este meticuloasă, metoda propusă de Lindner este o metodă precisă, deoarece se face sub control microscopic.
Metoda Naumov este folosită pentru izolarea culturilor pure de mucegaiuri. Dintr-o diluţie convenabilă se aplică distanţat micropicături peste care se adaugă picături de mediu MMA fluidificat (42°C) şi după 3-8 zile se selectează din picătura cu o singură colonie cultura pură dorită.
O metodă simplificată pentru separarea sporilor fungici constă în inundarea unei plăci cu MMA cu 1-2 cm3 din diluţia convenabilă. Sporii care au rămas ataşaţi de mediu vor da colonii izolate. În general mucegaiurile nu ridică probleme la izolare deoarece cresc sub formă de colonii mari pe diverse alimente şi pentru obţinerea în cultură pură se face repicarea de spori situaţi în centrul coloniei.
Metode de izolare cu ajutorul micromanipulatorului. Este o metodă precisă şi se realizează cu ajutorul unui aparat prevăzut cu tuburi capilare cu care se poate face selecţia celulelor dorite din preparate studiate la microscop. Cu ajutorul micromanipulatorului se poate face recoltarea de ascospori din celule ascogene şi este folosit în dirijarea proceselor de fuziunea protoplaştilor, pentru conjugare etc.
Metode biologice de obţinere a culturilor pure
Metodele biologice sunt foarte diverse şi se bazează pe proprietăţi fiziologice ale microorganismelor de izolat care să se diferenţieze clar de cele ale microorganismelor însoţitoare din acelaşi biotop. Uneori prin aceste metode se face izolarea unui grup cu caractere taxonomice apropiate şi apoi se face izolarea de culturi pure prin tehnici de răspândire sau prin folosirea mediilor selective.
O metodă biologică clasică este metoda Burri prin care se face separarea microorganismelor în funcţie de necesarul de oxigen pentru creştere. Dintr-un mediu natural se face inocularea în BCA termostatat la 42°C şi după uniformizare acesta se introduce într-un tub de sticlă prevăzut la un capăt cu dop de cauciuc. Prin răcire celulele sunt imobilizate în gel şi prin termostatare în funcţie de accesul oxigenului din aer, în zona tubului prevăzut cu dop de cauciuc se vor dezvolta bacterii anaerobe, intermediar bacterii microaerofile, iar în stratul de mediu la care aerul a pătruns prin dopul de vată al tubului, bacterii aerobe.
Prin metode biologice pot fi selectate bacteriile sporogene din medii naturale pe baza termorezistenţei deosebite a endosporilor. De exemplu, Bacillus subtilis se poate izola din infuzie de fân, deoarece endosporii rezistă la fierbere, în timp ce alte bacterii sunt distruse şi prin germinare trec în forme vegetative şi care prin înmulţire prin sciziune rămân asociate formând în 24 ore un voal cutat.
Numeroase metode de izolare se bazează pe introducerea în medii de cultură a unor substanţe chimice cu efect inhibitor asupra microorganismelor de care trebuie separată cultura dorită. De exemplu, prin introducerea de 0,02% actidionă are loc inhibarea dezvoltării drojdiilor aflate în amestec cu bacterii. Metoda este folosită pentru izolarea unor bacterii ce pot produce contaminarea drojdiilor folosite sub formă de culturi pure în industriile fermentative.
Importanţa practică a culturilor pure
Izolarea şi obţinerea culturilor pure , cunoaşterea cineticii de creştere prezintă o importanţă practică deosebită în următoarele domenii:
Identificarea, selecţionarea şi îmbunătăţirea proprietăţilor de biosinteză
Culturile pure sunt folosite pentru studiul proprietăţilor morfologie şi fiziologice, în scopul identificării, caracterizării şi stabilirii domeniului de utilizare a culturii. Sub formă de culturi pure microorganismele pot fi supuse unor tratamente fizico-chimice prin care se pot induce modificări genetice la nivelul acizilor nucleici, cu obţinerea de culturi mutante, din rândul cărora se face din nou selecţia tulpinilor performante.
Obţinerea culturilor starter în procese fermentative industriale
Pornind de la cultura pură, în biotehnologii alimentare prin cultivarea în medii adecvate se obţine cantitatea necesară de inocul/maia folosită drept cultură starter a procesului fermentativ.
Inoculul reprezintă un mediu nutritiv steril în care s-au înmulţit celule aparţinând unei culturi pure, aflată în etapa finală a creşterii exponenţiale. Cantitatea de inocul trebuie astfel calculată încât prin introducerea sa în mediul fermentativ steril, concentraţia în celule să asigure declanşarea rapidă a procesului. În funcţie de specificul biotehnologic este obligatorie asigurarea continuităţii în transfer pentru aprovizionarea cu inocul activ, la perioada solicitată de producţie.
Utilizarea culturilor pure în biotehnologii alimentare (la fabricarea berii, alcoolului, vinului, produse lactate acide, panificaţie etc.) permite obţinerea unor produse cu calitate constantă.
Curba de creştere a culturii microbiene
Prin inocularea de celule, aparţinând unei culturi pure, într-un mediu nutritiv steril se poate stabili dinamica de creştere prin studiul vitezei de acumulare a biomasei sau prin creşterea numărului de celule raportat la unitatea de volum a mediului. În condiţiile experimentale, dinamica multiplicării microorganismelor este bine cunoscută. Procesul evoluează într-o serie de faze succesive.
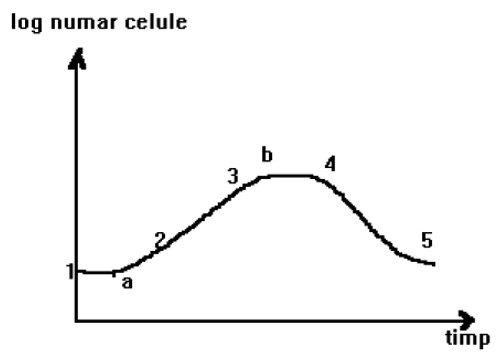
Fig.3. Curba de multiplicare a microorganismelor
1÷2-faza de repaos (faza lag);
1÷a-perioada de adaptare;
a÷2-perioada de refacere;
2÷3-faza exponenţială; 3÷4-faza staţionară;
3÷b- perioada de spor de creştere negativ;
b÷4-perioada de staţionare propriu-zisă;
5-faza finală de declin.
Faza de latenţă , de creştere zero sau de lag reprezintă etapa de timp când după inoculare numărul celulelor rămâne neschimbat, sau chiar scade, noile condiţii de mediu implică latenţa inducţiei acelor enzime necesare pentru adaptarea la mediul nutritiv. Faza de latenţă apare deci ca o perioadă de adaptare la condiţiile noi de cultură, în care microorganismele viabile din inocul îşi acumulează în celulă metaboliţi şi sistemele necesare creşterii, în cazul în care aceste componente biochimice le lipseau datorită condiţiilor de mediu anterioare inoculării.
În cazul drojdiilor această fază poate dura 1-2 ore,durată ce depinde de compoziţia mediului şi capacitatea de reglare a metabolismului propriu. Faza lag se poate prelungi mult dacă inoculul este obţinut din culturi vechi sau care s-au păstrat în condiţii de refrigerare. În schimb dacă la inoculare s-a folosit o cultură viguroasă, aflată în faza activă de creştere, în mediul cu o compoziţie similară, faza lag este scurtă sau poate să fie absentă.
Faza de multiplicare exponenţială sau de creştere logaritmică este caracterizată prin aceea că, după o scurtă perioadă (cca. 2 ore) de accelerare a ritmului de creştere, în care multiplicarea se produce cu o viteză progresivă mărită, acest ritm devine constant şi caracteristic în anumite condiţii de cultură, durata unei generaţii fiind minimă. Perioada de echilibru poate fi menţinută numai atât cât nu intervin alterări importante, pe care creşterea le poate provoca în compoziţia mediului.
De exemplu, numărul de celule de drojdie sau de bacterii şi cantitatea de materie vie formată creşte temporar după o progresie geometrică cu raţia 2. Celulele aflate în faza exponenţială de multiplicare sunt cele mai potrivite pentru cercetări de genetică şi fiziologie.
Faza staţionară (de maturare) în care numărul celulelor viabile este maxim şi rămâne constant o perioadă de timp. De exemplu, celulele de drojdie nu mai înmuguresc, îşi măresc volumul şi tind spre forma sferică, se rotunjesc. Celulele de microorganisme au în această fază caracteristicile morfologice cele mai tipice genului şi speciei. Această fază poate fi prelungită atunci când urmărim păstrarea culturii pure, prin modificarea unor factori care scad viteza de metabolism celular.
Faza de declin se caracterizează printr-o scădere în progresie geometrică în raport cu timpul a numărului de celule vii. Pe măsură ce mediul devine mai puţin favorabil, celulele vii nu se mai multiplică, deşi activitatea lor mai continuă un timp după care mor şi intră în autoliză. La sfârşitul acestei ultime faze se înregistrează maximum absolut al numărului total de celule formate pe parcursul întregii evoluţii a culturii.
Procedee de conservare a culturilor pure
Sub formă de culturi pure sunt păstrate microorganismele aflate în studiu şi care prezintă proprietăţi de biosinteză remarcabile, culturi întreţinute şi înregistrate în colecţii autorizate de microorganisme, denumite micoteci.
Dintre tehnicile aplicate pentru conservarea culturilor pure, tehnici bazate pe prelungirea fazei staţionare de creştere şi evitarea etapei de declin, se cunosc următoarele:
Repicarea periodică – prin transfer de celule din eprubeta cu cultura pură în care mediul nutritiv este epuizat, în eprubeta cu mediu nutritiv steril cu compoziţie similară. Intervalul de repicare este dependent de natura culturii, compoziţia mediului şi temperatura de păstrare. În timp ce bacteriile lactice necesită repicări la intervale de 1-3 săptămâni, drojdiile se pot păstra pe MMA 3-6 luni,iar bacteriile sporulate 6-12 luni.
Mucegaiurile sunt rezistente la păstrare şi chiar după uscarea mediului, sporii se menţin viabili ani de zile. Procedeul de repicare periodică necesită un mare volum de muncă, prezintă risc de contaminare şi este greu de realizat atunci când numărul de culturi de întreţinut este mare;
Prelungirea intervalului între două repicări – prin scăderea vitezei de metabolism a celulelor şi deci evitarea stării de declin ce poate duce la pierderea culturii se poate realiza prin:
- Menţinerea culturilor la temperaturi scăzute , în condiţii de refrigerare sau congelare. Culturile de fungi păstrate la 5°C se transferă anual, iar dacă păstrarea se face la 16°C la interval de 6 luni.
- Privarea de oxigen. În absenţa oxigenului din aer,microorganismele aerobe trec în stare latentă de viaţă. Pentru drojdii şi mucegaiuri, cultura dezvoltată în mediu solidificat (drept) se acoperă cu un strat de ulei de parafină steril. Când celulele vii se acoperă cu ulei de parafină (sterilizat în prealabil la 170°C, 2 ore) procesele metabolice ale fungilor decurg de10 ori mai lent.
- Reducerea umidităţii mediului conduce la trecerea celulelor în stare de anabioză care poate fi menţinută timp îndelungat fără a se produce modificări intracelulare, ireversibile. Bacteriile sporogene ale genului Bacillus se pot menţine sub formă de endospori prin antrenarea culturii în eprubete cu nisip steril şi după evaporarea apei sporii se menţin viabili, adsorbiţi pe nisip, zeci de ani.
Păstrarea culturilor în stare liofilizată.
Este tehnica cea mai utilizată şi avantajoasă, deoarece prelungeşte cel mai mult intervalul de conservare a culturilor, fără să producă modificări ale proprietăţilor lor fiziologice. În cazul mucegaiurilor, o suspensie de spori în lapte degresat se congelează rapid la - 25°C, apoi are loc uscarea în vacuum timp de trei ore în recipiente de sticlă care se închid ermetic şi culturile se pot menţine 10 ani. Spori aparţinând genului Aspergillus liofilizaţi şi păstraţi astfel la 7°C şi-au menţinut viabilitatea timp de 23 ani. Bacteriile lactice sunt mai sensibile la păstrare comparativ cu fungii.
Colecţii de culturi
În lume se cunosc colecţii de culturi care în marea lor majoritate cuprind culturi protejate prin brevete; dintre acestea colecţia NRRL – SUA cunoscută din 1975 cu acronym ARS cuprinde peste 1000 de tulpini în majoritatea lor de actinomicete şi mucegaiuri, CBS Fungus Collection – Olanda conţine 19300 fungi etc.
În cadrul Facultăţii de Ştiinţa şi Ingineria Alimentelor, Universitatea „Dunărea de Jos” din Galaţi există o micotecă cu acronym MIUG ce include tulpini de drojdii, mucegaiuri, bacterii.
Factori de control ai creşterii microorganismelor
Celula microbiană având o masă redusă este puternic influenţată de condiţiile mediului ambiant şi reacţionează foarte diferit la diferiţi factori, fie prin adaptare sau în caz contrar, prin dispariţie. Astfel creşterea microbiană este dependentă de numeroşi factori fizico-chimici şi biologici ceea ce a condus în cursul evoluţiei la adaptări specifice prin stabilirea de interrelaţii între microorganisme şi mediu.
Pentru a înţelege modul în care celula microbiană reacţionează la condiţiile mediului ambiant, diferiţi factori au fost împărţiţi în mod arbitrar în trei mari grupe, cu precizarea că, în condiţii naturale, bioefectul acestora poate fi cumulativ sau sinergic:
- Factori extrinseci sunt factori exogeni, ai mediului natural/industrial: temperatură, umezeală relativă a aerului, concentraţia de oxigen, radiaţii, factori mecanici, factori chimici etc.
- Factori intrinseci sunt factori dependenţi de natura alimentului care influenţează creşterea şi activitatea culturilor starter dar şi natura alterării specifice a produselor alimentare (compoziţia chimică şi concentraţia în nutrienţi, aw, pH, rH, structura anatomică, substanţe chimice etc.).
- Factori impliciţi sunt factori biologici determinaţi de relaţiile ce se pot stabili între diferitele grupe de microorganisme care alcătuiesc microbiota alimentului respectiv.