Suprarenalele
- Detalii
- Categorie: Endocrinologie
- Accesări: 6,523
Scurt istoric. 1550 - Leonardo da Vinci a desenat pentru prima dată suprarenalele fără a le denumi.
1563 - Bartolomeo Eustachius face prima descriere anatomică a suprarenalelor.
1856 - Brown Sequard a demonstrat rolul vital al suprarenalelor.
1930 - P. E. Smith a demonstrat existenţa axului hipofizo-corticosu- prarenal.
Topografia suprarenalelor
Suprarenalele sunt situate retroperitoneal, anterolateral de vertebrele 11, 12 toracale şi prima lombară, pe partea anteromedială a rinichilor. Uneori ţesut corticosuprarenal ectopic este decelat în rinichi, splină, paraaortal, bazin, uter, ovare, testicule. Rareori se nasc copii doar cu o suprarenală.
Corticosuprarenalele
Embriologie
Corticosuprarenalele se formează din mezodermul retroperitoneal începând cu săptămână a 6-8-a de gestaţie, dependenţa de ACTH fiind demonstrată la termenul de 10-20 săptămâni. La nou-născut se disting zona fetală (zona “X”), producătoare de dehidroepiandrosteron, care derivă în estrogeni, şi zona definitivă, care treptat, pe parcursul primului an de viaţă, înlocuieşte zona fetală.
Formarea definitivă a corticosuprarenalelor are loc pe parcursul primilor 3 ani de viaţă, fapt care explică subfebrilitatea întâlnită la unii copii de această vârstă. Suprarenalele continuă să crească până la vârsta postpubertară.
Aspectul macroscopic
Suprarenala dreaptă are aspect piramidal şi e mai groasă la mijloc decât cea stângă. Cea stângă are aspect semilunar. Lungimea fiecărei suprarenale este de 4 - 6 cm, lăţimea 2-3 cm, grosimea 1 cm, greutatea câte 4-5 grame. Corticosuprarenalele posedă capacitatea de a regenera.
Aspectul microscopic
Corticosuprarenala, care reprezintă 80 - 90% din glandă, include 3 zone active:
- Zona glomerulară , externă, sub capsula fibroasă, ocupă cca 15% din cortex, are conţinut celular de citoplasmă şi lipide, produce mineralo- corticoizi - aldosteron şi puţin dezoxicorticosteron (DOC).
- Zona fasciculată ocupă cca 75% din corticosuprarenală, fiind situată sub zona glomerulară. Este formată din celule bogate în lipide (clare) producătoare de glucocorticoizi şi puţini androgeni.
- Zona reticulata este situată sub zona fasciculată şi conţine celule bogate în granule, sărace în lipide producătoare de androgeni şi puţini estrogeni şi glucocorticoizi.
Vascularizarea. Alimentaţia cu sănge arterial este deosebit de intensă şi este asigurată în fiecare suprarenală prin 11-12 ramuri a 3 artere de la nivelul aortei, arterei renale sau frenice. După traversarea radială a suprarenalei, sângele se colectează în vena cavă inferioară (pe dreapta) şi vena renală (pe stânga).
Inervaţia simpatică se realizează prin ramurile toraco-lombare, iar cea parasimpatică prin ramurile vagale.
Biosinteza hormonilor corticosuprarenali debutează prin conversia colesterolului şi se numeşte steroidogeneză (vezi schema de mai jos).
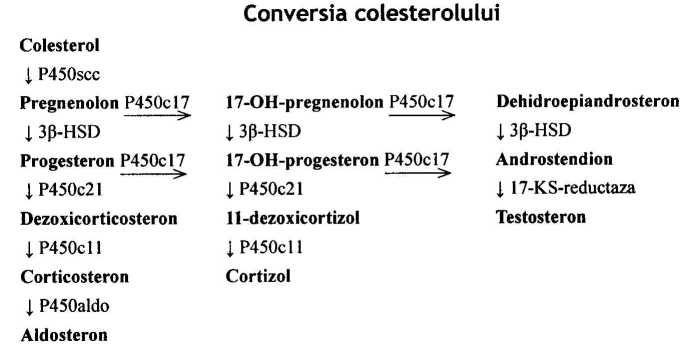
Biosinteza corticosteroizilor:
- P450scc - fermentul scindării lanţului lateral (desmolaza);
- P450cl7 - 17a-hidroxilaza/17,20-liaza;
- 3|3-HSD - hidroxisteroiddehidrogenaza;
- P450c21 - 21-hidroxilaza;
- P450cll - llp-hidroxilaza;
- P450aldo - aldosteronsintetaza.
Colesterolul, preluat 70 - 80% din lipoproteidele circulante şi 20 - 30% sintetizat în corticosuprarenale, derivă în mitocondrii sub acţiunea a 3 enzi- me, formând pregnenolon (vezi schema 1) care transformându-se pe 3 căi sub acţiunea enzimelor din familia citocrom P 450 oxigenazelor, generează:
- în zona glomerulară, preponderent mineralocorticoizi (aldosteron, DOC);
- în zona fasciculată, preponderent glucocorticozi (cortizol);
- în zona reticulată - hormoni sexuali: dehidroepiandrosteron (DHEA), dehidroepiandrosteron-sulfat (DHEAS), androstendion, testosteron, estron, estradiol.
Circulaţia sanguină
Circa 50% din aldosteron prezintă o fracţie legată cu proteinele, în special cu album inele, printr-o legătură slabă. DOC este un mineralocorticoid puternic, 95% din care este legat de proteinele plasmatice şi nu este biologic activ.
Din 90 - 93%, cortizolui seric este legat cu proteinele în special cu CBG (corticoid-binding-globulin, transcortină), iar 10 - 15% cu albuminele si alte proteine. Cresc nivelul CBG şi inactivează cortizolui seric estrogenii, contraceptivele orale, hormonii tiroidieni, hiperglicemia, sarcina. Scad nivelul CBG glucocortieoizii, insuficienţa hepatică, renală, tiroidiană, factorii genetici. 90% din DHEA şi androstendion sunt legate slab cu proteinele. 98% din testosteron şi DHEAS al steroizilor corticosuprarenali sunt legate strâns cu globul inele.
Metabolismul şi excreţia
Transformarea steroizilor corticosuprarenali în produşi hidrosolubili are loc în ficat, 90% fiind apoi eliminaţi cu urina. Aldosteronul, care are un timp de înjumătăţire plasmatic sub 15 minute, este hidroxilat până la tetra- şi hexahidroaidosteron şi excretat preponderent cu urina. Doar 1% din aldosteron este eliminat în formă liberă de către rinichi.
Cortizolul cu timpul de înjumătăţire plasmatică de 70 - 120 minute, este hidroxilat în ficat cu formare de tetra- şi hexahidrocortizol, fiind glicurono- conjugat şi eliminat Ia nivel renal ca 17 hidroxicorticosteroizi (17 - OH CS). în 24 ore 70% din cortizol se elimină cu urina şi 30% prin tractul digestiv.
Androgenii sunt convertiţi, în special, la nivelul celulelor ţintă în androgeni mai activi: testosteron şi dehidrotestosteron, apoi hidroxilaţi şi conjugaţi în ficat, fiind eliminaţi cu urina ca 17 ketosteroizi (17- K.S: androsteron, etiocolanolon, DHEA -sulfat). Inactivarea şi eliminarea testosteronului şi a aldosteronului este de 2 -3 ori mai activă la bărbaţi, posibil sub influenţa hormonilor gonadali steroizi asupra globulinelor plasmatice.
Acţiunile steroizilor corticosuprarenali
Mineralocortocoizii stimulează la nivel renal (mai puţin salivar, sudo- ripar, intestinal) reabsorbţia de Na şi eliminarea de K, H, Ca, Mg. Astfel creşte retenţia de apă şi volumul de lichid extracelular.
Glucocorticoizii influenţează metabolismele şi ţesuturile.
Metabolismul glucidic - creşte neoglucogeneza, inclusiv prin catabolis- mul proteic şi lipidic, reduce captarea glucozei de către celule (rezistenţă insulinică).
Metabolismul proteic - stimulează proteoliza, inhibă anabolismul proteic.
Metabolismul lipidic - creşte lipoliza şi eliberarea de acizi graşi, ce- toacidoza, stimulează lipogeneza selectivă, indirectă prin apetit crescut şi hiperinsulinism.
Metabolismul calciului - inhibă absorbţia intestinală de Ca, creşte conţinutul de vit. D şi fosfor, stimulând parathormonul.
Ţesutul osos - stimulează osteoclastele şi acţiunea PTH, producînd osteoporoză.
Ţesutul conjunctiv - stimulează pierderea de colagen, inhibă fibroblaştii.
Creşterea este stimulată în cantităţi fiziologice; în exces - blochează somatomedinele, GH şi creşterea.
Hematopoieza - stimulează eritropoieza.
Leucopoieza - creşte leucocitoza, provoacă eozino-, limfopenie, neu- trofilie.
Sistemul imun - inhibă răspunsul imun şi infiamatoriu, histamina, sero- tonina, bradichinina.
Aparatul cardiovascular - creşte tensiunea arterială, presiunea intraoculară.
Aparatul digestiv - creşte secreţia gastrică, uneori ulcere peptice - steroide.
Rinichii - stimulează fluxul sanguin renal şi filtraţia glomerulară.
Sistemul nervos central - în cantităţi fiziologice, exercită acţiune stimulatoare, fiind hormon de răspuns la stres. Deficienţa generează astenie, depresie. Excesul induce euforie, apoi depresie, uneori suicid.
Sistemul endocrin. Produce feed-back negativ a secreţiei de CRH şi ACTH. Inhibă răspunsul TSH-ului la TRH şi conversia de tiroxină în triiodtironină. Inhibă răspunsul LH şi FSH la LH-RH, GH şi scade GH.
Androgenii
La copii, inclusiv la fete, iniţiază şi stimulează pubertatea prin axul gonadotrop.
La femei stimulează pilozitatea sexual dependentă (axilo-pubiană), libidoul, fiind şi o sursă suplimentară de estrogeni după aromatizarea din ţesutul adipos.
La bărbaţi au rol secundar în menţinerea caracterelor sexuale secundare şi stimularea comportamentului sexual (comparativ cu cei testiculari).
Controlul secreţiei corticosuprarenalelor
Zona glomerulară este practic independentă de ACTH şi este stimulată de sistemul renină-angiotensină la hiponatriemie, hiperkaliemie, hipoten- siune, vasodilatare, ortostatism.
Zona fasciculată este stimulată de ACTH prin:
-
mecanism feed-back negativ lung, scurt, ultrascurt;
-
sistemul serotoninergic de la nivelul nucleului arcuat, care asigură ritmul nictemeral al secreţiei de ACTH;
-
sistemul de răspuns la stres modulat de hipotalamus şi cu creştere evidentă a cortizolului;
-
ritmul circadian al secreţiei de ACTH, urmată peste 2-3 minute şi de creşterea producerii de cortizol cu valori maximale la 6 - 8 dimineaţa şi minimale la 22 - 24.
Circa 80% din cortizol este secretat exploziv, periodic la 40 minute - 6 ore în a doua jumătate a zilei.
Zona reticulata se află sub controlul ACTH, dar androgenii nu sunt in- plicaţi în controlul secreţiei de ACTH.
ACTH-ul stimulează troficitatea şi steroidogeneza acţionînd, în special, la nivelul transformării iniţiale a colesterolului în pregnenolon.
Medulosuprarenalele
Scurt istoric. în 1805 Cuvier diferenţiază pentru prima dată medulo- de corticosuprarenală.
în 1904 şi 1907 au fost sintetizate pentru prima dată noradrenalina şi adrenalina.
Emhriologia medulosuprarenalelor
Medulosuprarenalele se formează începînd cu a 6 săptămână a vieţii intrauterine dintr-un grup de celule cromafine ale crestei neurale. Semne de activitate secretorie se înregistrează din săptămâna a 12-a.
Structura macroscopică
Stratul medular este închis în suprarenală de către zona reticulară a corticosuprarenalei fără o demarcaţie clară. Greutatea ambelor medulosu- prarenale e de cca 1 gram.
Inervaţia se face prin fibrele paraganglionare ale sistemului nervos simpatic.
Alimentaţia sanguină este comună cu cea a corticosuprarenalelor.
Structura microscopică
Medulosuprarenala conţine celule cromafine, numite feocromocite (“pheo”- brună, după culoarea granulaţiilor la oxidarea noradrenalinei şi a adrenalinei în melanină sub acţiunea bicromatului de potasiu). Multiplele granule celulare cromafine au rol important atât în secreţia, cât şi în stocarea catecolaminelor.
Biosinteza
în medulosuprarenale are loc formarea catecolaminelor, numite astfel datorită nucleului catecolic (3-4 dioxifenilic) din moleculă.
Tirozina din alimente şi din fenilalanina hepatică se transformă sub influenţa enzimei tirozinhidroxilaza în dihidroxifenilalanină (DOPA), apoi în dopamină (DA) sub acţiunea dopadecarboxilazei, iar aceasta în noradrenalină (NA) sub influenţa dopamin-beta-hidroxilazei. Noradrenalina, la rândul ei, sub acţiunea feniletanolamin-N-metiltransferazei indusă de glucocorticoizi este transformată în adrenalină (A). Suprarenalele omului conţin preponderent adrenalină (80 - 90%).
Stocarea
Catecolaminele se stochează în granule împreună cu ATP, peptide active, VIP (peptidul vasoactiv intestinal), ACTH, encefaline, menţinând osmolaritatea necesară.
Secreţia
Secreţia este stimulată neurogen prin acetilcolina terminaţiilor fibrelor preganglionare simpatice. Efect stimulatoriu au impulsurile la nivel de receptor prin:
- up- şi down-regulation;
- receptorii beta (în special pentru noradrenalină);
- stres (în special pentru noradrenalină);
- pătrunderea Ca în celulă cu stimularea exocitozei.
Metabolismul este activ, ţinînd cont de perioada de înjumătăţire foarte scurtă a catecolaminelor.
Căile de metabolizare sunt:
- eliminarea prin rinichi (cca 5% din catecolamine);
- reincluderea celulară a unor produşi intermediari cu completarea rezervelor de catecolamine;
- descompunerea în ficat pe calea metoxilării sub influenţa catecol-O- metil-transferazei (COMT) cu formare de metanefrină şi normetane- ffină, iar apoi sub influenţa MAO şi a aldehidoxidazei trec în acid vanil-mandelic (AVM);
- din oxidarea sub acţiunea primară a mono-amino-oxidazei, evitând COMT, rezultă la fel acidul vanil-mandelic - produsul principal al descompunerii.
Efectele fiziologice sunt realizate prin intermediul receptorilor adre- nergici α1, α2 (β1, β2 rezultatul final fiind determinat de afinitatea diferită a ţesuturilor la adrenalină şi noradrenalină:
- stimularea cardiacă globală(conductibilitatea, contractibilitatea, frecvenţa (β1,);
- vasoconstricţie subcutanată, renală, splanhică, hipertensiune arterială;
- vasodilatare în cord, creier, musculatura striată, bronhodilatare, mi- driază (β 2);
- activarea glicogenolizei hepatice, generând hiperglicemie (α1, β 2);
- creşterea glicogenolizei din muşchii scheletici cu lactacidoză (β 2);
- stimularea lipolizei cu formare de AGL, glicerină, cetoacidoză (β,);
- hipersudoraţie, contracţii bronşice, uterine, ejaculare (α1,).