ADN - Acidul dezoxiribonucleic
- Detalii
- Categorie: Biochimie
- Accesări: 1,460
Acidul dezoxiribonucleic, cunoscut sub acronimul ADN (sau DNA în engleză), reprezintă o macromoleculă de o importanță covârșitoare pentru toate organismele vii de pe planeta noastră. Această moleculă remarcabilă poartă informația genetică necesară pentru dezvoltarea, funcționarea și reproducerea tuturor formelor de viață cunoscută. Mai simplu spus, ADN-ul este limbajul de programare al vieții, un cod universal care dictează tot ceea ce suntem din punct de vedere biologic.
În fiecare celulă din corpul uman (cu excepția celulelor roșii din sânge), ADN-ul este prezent, conținând instrucțiunile precise pentru construirea proteinelor care, la rândul lor, determină structura și funcțiile organismului nostru. De la culoarea ochilor până la predispoziția către anumite boli, ADN-ul influențează toate aspectele biologice ale existenței noastre.
Acest articol vă va ghida printr-o călătorie fascinantă în universul ADN-ului, explorând structura sa chimică unică, funcțiile esențiale, modul în care se transmite informația genetică, precum și aplicațiile moderne în medicină, criminalistică și cercetarea științifică. Vom descoperi împreună cum o moleculă aparent simplă conține secretele vieții așa cum o cunoaștem.
Structura Chimică a ADN-ului: O Capodoperă Moleculară
Pentru a înțelege importanța și funcțiile ADN-ului, trebuie să începem cu structura sa fundamentală. ADN-ul este un polimer format din unități repetitive numite nucleotide, care se leagă între ele formând două lanțuri lungi care se răsucesc unul în jurul celuilalt într-o configurație unică numită dublă elice.
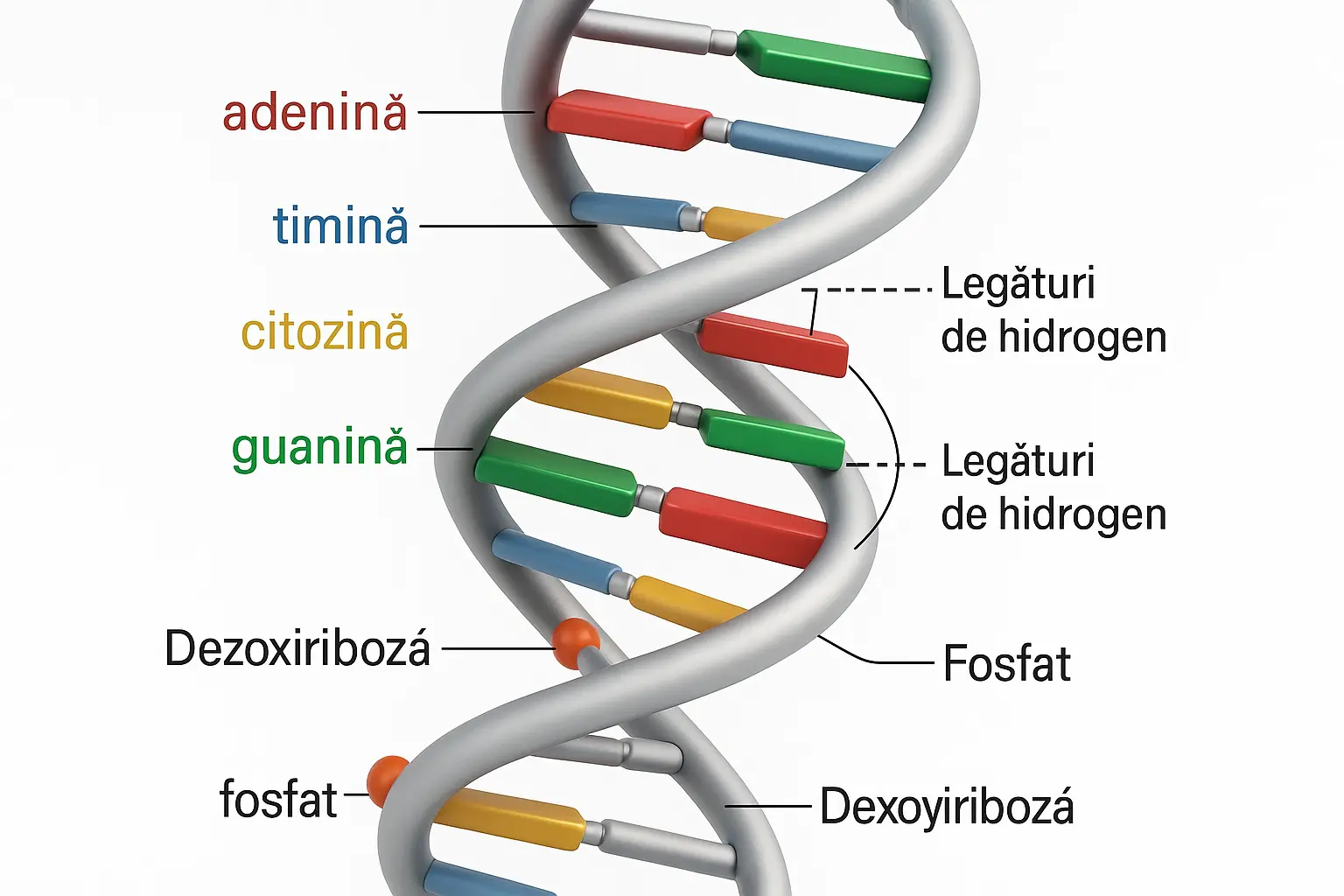
Nucleotidele: Cărămizile Fundamentale
Fiecare nucleotidă este compusă din trei componente esențiale:
-
O moleculă de dezoxiriboză - un zahar cu cinci atomi de carbon (pentoza) care formează "coloana vertebrală" a ADN-ului.
-
O grupare fosfat - un grup funcțional derivat din acid fosforic, care leagă moleculele de zahar între ele.
-
O bază azotată - componentă care conține azot și care diferențiază nucleotidele între ele.
Bazele Azotate și Codul Genetic
ADN-ul conține patru tipuri diferite de baze azotate, care reprezintă "literele" codului genetic:
- Adenina (A) - o bază purinică cu două inele
- Guanina (G) - o bază purinică cu două inele
- Citozina (C) - o bază pirimidinică cu un singur inel
- Timina (T) - o bază pirimidinică cu un singur inel
Aceste baze se împerechează specific: adenina formează întotdeauna pereche cu timina (prin două legături de hidrogen), iar guanina formează întotdeauna pereche cu citozina (prin trei legături de hidrogen). Această împerechere specifică, numită "complementaritate", este esențială pentru funcțiile ADN-ului, inclusiv replicarea și transcripția.
Dubla Elice: O Structură Revoluționară
În 1953, James Watson și Francis Crick, folosind datele de difracție cu raze X obținute de Rosalind Franklin și Maurice Wilkins, au propus modelul dublei elice pentru ADN. Această structură elegantă și funcțională explică perfect cum poate ADN-ul să stocheze și să transmită informația genetică.
În această configurație:
- Cele două lanțuri polinucleotidice sunt orientate în direcții opuse (antiparalel).
- Bazele azotate sunt orientate spre interiorul elicei.
- Scheletul zahăr-fosfat formează partea exterioară a structurii.
- Elica completă face o rotație completă la aproximativ 10-11 perechi de baze.
| Proprietate | Valoare | Semnificație biologică |
|---|---|---|
| Diametrul dublei elice | 2 nanometri | Permite impachetarea eficientă în cromozomi |
| Distanța între perechi de baze | 0,34 nanometri | Stabilizează structura prin interacțiuni de stivuire |
| Perechi de baze per rotație | 10,5 | Determină forma B a ADN-ului (forma predominantă) |
| Lățimea șanțului major | 22 Å | Permite interacțiunea cu proteine reglatoare |
| Lățimea șanțului minor | 12 Å | Accesibil pentru molecule mici care se leagă de ADN |
| Lungimea ADN-ului uman complet | ~2 metri | Trebuie compactat de 10.000 de ori pentru a încăpea în nucleu |
Replicarea ADN-ului: Perpetuarea Codului Vieții
Una dintre cele mai remarcabile proprietăți ale ADN-ului este capacitatea sa de a se autoreplica, permițând transmiterea informației genetice de la o generație la alta. Acest proces complex, dar incredibil de precis, asigură că fiecare celulă nouă primește o copie identică a materialului genetic.
![]()
Mecanismul Replicării Semiconservative
Replicarea ADN-ului este semiconservativă, ceea ce înseamnă că fiecare moleculă de ADN nou formată conține un lanț din molecula parentală (conservat) și un lanț nou sintetizat. Acest mecanism a fost confirmat experimental de Meselson și Stahl în 1958.
Procesul de replicare implică mai multe etape și enzime specializate:
-
Desfacerea dublei elice: Enzima helicase desface legăturile de hidrogen dintre bazele complementare, separând cele două lanțuri ale ADN-ului.
-
Stabilizarea ADN-ului monocatenar: Proteine specializate se atașează de ADN-ul monocatenar pentru a preveni reasocierea lanțurilor.
-
Sinteza ADN-ului: ADN polimeraza adaugă nucleotide complementare bazelor de pe lanțul matriță, respectând regula de împerechere (A-T, G-C).
-
Sinteza discontinuă: Pe lanțul întârziat (lagging strand), sinteza ADN-ului are loc în direcție opusă progresiei furcii de replicare, rezultând fragmente scurte numite fragmente Okazaki.
-
Procesarea fragmentelor: Primerele de ARN sunt înlocuite cu ADN, iar fragmentele sunt unite prin intermediul enzimei ADN ligaza.
| Etapă | Enzimă principală | Funcție |
|---|---|---|
| Desfacerea dublei elice | Helicase | Separă cele două lanțuri ale ADN-ului |
| Stabilizarea lanțurilor | Proteine SSB | Previne reasocierea prematură a lanțurilor |
| Sinteza primerului | Primază | Sintetizează scurte fragmente de ARN ca punct de start |
| Sinteza ADN-ului | ADN polimerază | Adaugă nucleotide complementare la lanțul în creștere |
| Eliminarea primerilor | ADN polimerază I | Îndepărtează primerii de ARN și îi înlocuiește cu ADN |
| Legarea fragmentelor | ADN ligază | Unește fragmentele de ADN pentru a forma un lanț continuu |
Fidelitatea replicării ADN-ului este remarcabilă, cu o rată de eroare de aproximativ 1 la 10⁹-10¹⁰ nucleotide. Această precizie este asigurată de mecanismele de verificare (proofreading) ale ADN polimerazei și de sistemele de reparare post-replicativă.
De la ADN la Proteine: Fluxul Informației Genetice
Informația stocată în ADN trebuie să fie "citită" și utilizată pentru a ghida funcțiile celulare. Acest proces, cunoscut sub numele de expresie genică, implică două etape principale: transcripția și traducerea.
Transcripția: De la ADN la ARN
În procesul de transcripție, informația genetică din ADN este copiată într-o moleculă de ARN (acid ribonucleic) mesager (ARNm). ARN-ul diferă de ADN prin:
- Conține riboza în loc de dezoxiriboză
- Utilizează uracilul (U) în loc de timină (T)
- Este, de obicei, monocatenar
Transcripția are loc în nucleul celulelor eucariote și implică mai multe etape:
- Inițierea: ARN polimeraza se leagă de o regiune promotor din ADN.
- Elongația: ARN polimeraza sintetizează ARNm complementar uneia dintre catenele ADN-ului (catena antisens).
- Terminarea: Transcripția se oprește când ARN polimeraza întâlnește o secvență de terminare.
În celulele eucariote, ARNm-ul trebuie să fie procesat înainte de a părăsi nucleul, prin:
- Adăugarea unei "căciulițe" (cap) la capătul 5'
- Adăugarea unei cozi poli-A la capătul 3'
- Eliminarea intronilor (secvențe necodificatoare) și unirea exonilor (secvențe codificatoare) - proces numit splicing
Traducerea: De la ARN la Proteine
După procesare, ARNm-ul părăsește nucleul și se deplasează spre ribozomi, unde informația sa va fi tradusă în secvențe de aminoacizi care formează proteine.
Traducerea implică:
- Codul genetic: Secvența de nucleotide din ARNm este "citită" în grupuri de câte trei, numite codoni. Fiecare codon specifică un anumit aminoacid sau un semnal de oprire.
- ARN de transfer (ARNt): Molecule care transportă aminoacizii specifici și conțin anticodoni complementari codonilor din ARNm.
- Ribozomi: Structuri celulare complexe care facilitează legarea ARNt-urilor la ARNm și formarea legăturilor peptidice între aminoacizi.
| Codon (ARNm) | Aminoacid | Codon (ARNm) | Aminoacid | Codon (ARNm) | Aminoacid | Codon (ARNm) | Aminoacid |
|---|---|---|---|---|---|---|---|
| UUU, UUC | Fenilalanină | UCU, UCC, UCA, UCG, AGU, AGC | Serină | UAU, UAC | Tirozină | UGU, UGC | Cisteină |
| UUA, UUG, CUU, CUC, CUA, CUG | Leucină | CCU, CCC, CCA, CCG | Prolină | CAU, CAC | Histidină | CGU, CGC, CGA, CGG, AGA, AGG | Arginină |
| AUU, AUC, AUA | Izoleucină | ACU, ACC, ACA, ACG | Treonină | AAU, AAC | Asparagină | GUU, GUC, GUA, GUG | Valină |
| AUG | Metionină (Start) | GCU, GCC, GCA, GCG | Alanină | GAU, GAC | Acid aspartic | GGU, GGC, GGA, GGG | Glicină |
| UAA, UAG, UGA | Stop | AAA, AAG | Lizină | GAA, GAG | Acid glutamic | ||
| CAA, CAG | Glutamină | UGG | Triptofan |
O caracteristică importantă a codului genetic este că este degenerat: mai mulți codoni pot specifica același aminoacid. Această redundanță oferă o anumită protecție împotriva efectelor mutațiilor.
Mutații și Variabilitate Genetică: Motorul Evoluției
Mutațiile sunt modificări ale secvenței nucleotidice a ADN-ului. Ele reprezintă sursa primară a variabilității genetice și, prin urmare, materia primă pentru selecția naturală și evoluție.
Tipuri de Mutații
-
Mutații punctiforme:
- Substituții: Înlocuirea unei baze cu alta (de exemplu, A → G)
- Tranziții: Substituții între purine (A ↔ G) sau între pirimidine (C ↔ T)
- Transversii: Substituții între o purină și o pirimidină (de exemplu, A → C)
-
Mutații structurale:
- Deleții: Pierderea uneia sau mai multor baze
- Inserții: Adăugarea uneia sau mai multor baze
- Duplicații: Copierea unei secvențe de ADN
- Inversii: Răsturnarea orientării unei secvențe de ADN
- Translocații: Mutarea unei secvențe de ADN într-o altă locație
-
Efectele mutațiilor asupra proteinelor:
- Mutații silențioase: Nu modifică aminoacidul codificat
- Mutații missense: Schimbă un aminoacid cu altul
- Mutații nonsense: Introduc un codon de stop prematur
- Mutații frameshift: Modifică cadrul de citire, afectând toți aminoacizii din aval
| Tip de mutație | Mecanismul | Exemplu | Potențial efect |
|---|---|---|---|
| Substituție silențioasă | Schimbarea unui codon cu altul care specifică același aminoacid | GGA → GGG (ambele codează glicină) | Niciun efect asupra proteinei |
| Substituție missense | Schimbarea unui codon cu altul care specifică un aminoacid diferit | GAG (Glu) → GTG (Val) | Poate afecta funcția proteinei, în funcție de importanța aminoacidului |
| Substituție nonsense | Schimbarea unui codon care specifică un aminoacid cu un codon stop | CAG (Gln) → TAG (Stop) | Truncarea proteinei, adesea cu pierderea funcției |
| Inserție/deleție | Adăugarea sau eliminarea de nucleotide care nu sunt multipli de trei | Inserția unei singure baze | Modificarea cadrului de citire, afectând toți aminoacizii din aval |
| Duplicație | Copierea unei secvențe de gene | Duplicarea genei pentru receptorul de culoare roșie | Poate duce la exprimarea crescută sau la noi funcții prin evoluție |
Tehnologii Moderne Bazate pe ADN: De la Laborator la Viața Cotidiană
Înțelegerea structurii și funcțiilor ADN-ului a condus la dezvoltarea unor tehnologii revoluționare care au impact în medicină, agricultură, criminalistică și multe alte domenii.
Secvențierea ADN-ului
Secvențierea ADN-ului este procesul de determinare a ordinii exacte a nucleotidelor într-o moleculă de ADN. Metodele moderne permit secvențierea rapidă și la costuri din ce în ce mai reduse a genomurilor complete.
- Metoda Sanger: Prima metodă eficientă de secvențiere, bazată pe terminatori de lanț dideoxinucleotidici.
- Secvențierea de nouă generație (NGS): Metode moderne care permit secvențierea paralelă a milioane de fragmente de ADN.
- Secvențierea nanopore: Tehnologie care permite secvențierea în timp real a unor molecule lungi de ADN.
Reacția în Lanț a Polimerazei (PCR)
PCR este o tehnică care permite amplificarea exponențială a unei secvențe specifice de ADN, generând milioane de copii în câteva ore. Această metodă, dezvoltată de Kary Mullis în anii 1980, a revoluționat biologia moleculară și are nenumărate aplicații, de la diagnosticul bolilor până la criminalistică.
| Etapă PCR | Temperatură | Durată | Proces |
|---|---|---|---|
| Denaturare | 94-98°C | 20-30 secunde | Separarea lanțurilor de ADN |
| Hibridizarea primerilor | 50-65°C | 20-40 secunde | Atașarea primerilor la ADN-ul țintă |
| Extensie | 72°C | 1-2 minute | Sinteza noilor lanțuri de ADN |
| Repetarea ciclului | - | - | De obicei 25-35 de cicluri |
CRISPR-Cas9: Revoluția Editării Genomice
CRISPR-Cas9 reprezintă o tehnologie de editare genomică care permite modificarea precisă a secvențelor de ADN. Sistemul utilizează o enzimă (Cas9) ghidată de o moleculă de ARN pentru a ținti și modifica secvențe specifice de ADN.
Aplicațiile CRISPR-Cas9 includ:
- Corectarea mutațiilor care cauzează boli genetice
- Crearea animalelor model pentru studiul bolilor
- Dezvoltarea culturilor agricole cu caracteristici îmbunătățite
- Investigarea funcțiilor genelor
ADN-ul în Criminalistică
Profilele ADN au revoluționat criminalistică, oferind o metodă extrem de precisă pentru identificarea persoanelor. Această tehnică se bazează pe analiza regiunilor hipervariabile ale ADN-ului, cunoscute sub numele de STR (Short Tandem Repeats).
Aplicațiile ADN-ului în criminalistică includ:
- Identificarea suspecților pe baza probelor biologice de la locul crimei
- Stabilirea relațiilor de paternitate
- Identificarea victimelor dezastrelor în masă
- Exonerarea persoanelor condamnate pe nedrept
ADN-ul în Sănătate și Boală: Implicații Medicale
Înțelegerea rolului ADN-ului în sănătate și boală a deschis noi perspective în diagnosticul, prevenția și tratamentul afecțiunilor medicale.
Boli Genetice
Bolile genetice sunt cauzate de mutații în una sau mai multe gene. Acestea pot fi:
- Monogenice: Cauzate de mutații într-o singură genă (de exemplu, fibroza chistică, anemia falciformă)
- Poligenice: Implică interacțiuni complexe între mai multe gene (de exemplu, diabetul de tip 2, hipertensiunea arterială)
- Cromozomiale: Rezultă din anomalii ale numărului sau structurii cromozomilor (de exemplu, sindromul Down)
| Boală genetică | Tip | Mutație | Prevalență | Manifestări clinice principale |
|---|---|---|---|---|
| Fibroza chistică | Monogenică (AR) | Genă CFTR | 1:2.500-3.500 nașteri la caucazieni | Infecții pulmonare cronice, insuficiență pancreatică |
| Hemofilia A | Monogenică (X-linkată) | Genă F8 | 1:5.000-10.000 băieți | Sângerări prelungite, hematoame |
| Sindromul Down | Cromozomială | Trisomia 21 | 1:700 nașteri | Dizabilitate intelectuală, trăsături faciale distinctive |
| Boala Huntington | Monogenică (AD) | Genă HTT (expansiune CAG) | 1:10.000-20.000 | Mișcări involuntare, declin cognitiv, tulburări psihiatrice |
| Cancerul de sân ereditar | Monogenică (AD) | Gene BRCA1/BRCA2 | 5-10% din cazurile de cancer de sân | Risc crescut de cancer de sân și ovarian |
AR = autosomal recesiv, AD = autosomal dominant
Medicina Genomică și Medicina de Precizie
Medicina genomică utilizează informațiile din genomul unui individ pentru a personaliza prevenția, diagnosticul și tratamentul bolilor.
Aplicații ale medicinei genomice:
- Testare genetică: Identificarea mutațiilor asociate cu boli genetice
- Farmacogenomică: Adaptarea tratamentelor medicamentoase la profilul genetic al pacientului
- Screeningul neonatal: Identificarea precoce a bolilor genetice tratabile
- Terapia genică: Corectarea mutațiilor genetice la nivel celular
ADN-ul și Evoluția: Dovezi Moleculare ale Originii Comune
ADN-ul oferă dovezi puternice pentru teoria evoluției și originea comună a tuturor organismelor vii.
Filogenie Moleculară
Compararea secvențelor de ADN între diferite specii permite reconstruirea relațiilor evolutive și estimarea timpului de divergență între linii. Gene conservate, precum cele care codifică ARN-ul ribozomal, sunt deosebit de utile în acest sens.
ADN-ul Mitocondrial și Cromozomul Y
ADN-ul mitocondrial (transmis pe linie maternă) și regiunile specifice ale cromozomului Y (transmise pe linie paternă) permit studierea migrațiilor umane și reconstruirea istoriei populațiilor.
Schimbările în Genom și Adaptarea
Studierea variațiilor genomice în populații permite identificarea selecției naturale în acțiune și înțelegerea bazei genetice a adaptărilor la diferite medii.
Provocări Etice și Sociale în Era Genomică
Progresele în tehnologiile ADN ridică numeroase întrebări etice, legale și sociale care necesită atenția societății.
Confidențialitatea Datelor Genetice
Informațiile genetice sunt extrem de personale și pot dezvălui detalii sensibile despre:
- Riscul de a dezvolta anumite boli
- Relațiile familiale
- Originea etnică
Protejarea confidențialității acestor date reprezintă o provocare importantă în era genomică.
Discriminarea Genetică
Există preocupări legate de potențiala discriminare pe baza informațiilor genetice în:
- Asigurări de sănătate și de viață
- Angajare
- Educație
Multe țări au adoptat legislație pentru a preveni discriminarea genetică, precum Genetic Information Nondiscrimination Act (GINA) în SUA.
Editarea Genomului Uman
Tehnologiile de editare genomică precum CRISPR-Cas9 ridică întrebări profunde despre limitele intervenției în genomul uman:
- Este etic să modificăm genomul embrionilor umani?
- Cum trasăm linia între tratarea bolilor și "îmbunătățirea" genetică?
- Cine ar trebui să aibă acces la aceste tehnologii?
Biobancarea și Utilizarea Secundară a Eșantioanelor
Colectarea și stocarea eșantioanelor biologice și a datelor genetice ridică întrebări despre:
- Consimțământul informat
- Beneficiile comerciale derivate din cercetare
- Drepturile participanților la cercetare
Viitorul Cercetării ADN-ului: Perspective și Promisiuni
Cercetarea ADN-ului continuă să evolueze rapid, deschizând noi orizonturi în știință și medicină.
Genomica Funcțională și Sisteme Biologice
Înțelegerea funcției tuturor genelor și a interacțiunilor complexe dintre ele reprezintă o prioritate a cercetării moderne. Genomica funcțională integrează date din transcriptomică, proteomică și metabolomică pentru a construi o imagine holistică a funcționării celulei.
Epigenomica
Modificările epigenetice - schimbări în expresia genică care nu implică modificări ale secvenței ADN - reprezintă un domeniu de cercetare în plină expansiune. Acestea includ metilarea ADN-ului, modificările histonelor și ARN-urile necodificatoare.
ADN-ul Sintetic și Biologia Sintetică
Capacitatea de a sintetiza secvențe de ADN din nucleotide și de a crea genomi artificiali deschide perspective fascinante pentru:
- Crearea de microorganisme cu funcții noi
- Producerea de biocombustibili și biomateriale
- Dezvoltarea de tratamente medicale personalizate
ADN-ul ca Mediu de Stocare a Datelor
Densitatea informațională remarcabilă a ADN-ului (1 gram poate stoca teoretic până la 455 exabytes de date) face din această moleculă un potențial mediu de stocare a datelor digitale pe termen lung.
Întrebări Frecvente despre ADN
1. Ce este ADN-ul și de ce este important?
ADN-ul (acid dezoxiribonucleic) este o macromoleculă care stochează informația genetică necesară pentru dezvoltarea, funcționarea și reproducerea organismelor vii. Este esențial pentru toate formele de viață.
2. Cum este structurată molecula de ADN?
ADN-ul are o structură de dublă elice, alcătuită din două lanțuri de nucleotide. Fiecare nucleotidă conține o dezoxiriboză, o grupare fosfat și o bază azotată (A, T, C, G).
3. Ce înseamnă replicarea semiconservativă a ADN-ului?
Replicarea semiconservativă înseamnă că fiecare moleculă nouă de ADN conține un lanț original și unul nou sintetizat. Acest proces asigură transmiterea fidelă a informației genetice.
4. Care este diferența dintre transcripție și traducere în expresia genică?
Transcripția este procesul prin care ADN-ul este copiat într-un ARN mesager. Traducerea este etapa în care acest ARNm este folosit pentru a sintetiza o proteină pe baza codului genetic.
5. Ce aplicații moderne are ADN-ul în medicină și criminalistică?
ADN-ul este folosit în testarea genetică, diagnosticul bolilor, medicina personalizată, identificarea persoanelor în criminalistică și stabilirea paternității.
Concluzie: ADN-ul, O Moleculă cu Impact Nemăsurat
Acidul dezoxiribonucleic reprezintă mult mai mult decât o simplă moleculă biologică. Este purtătorul codului vieții, legătura dintre toate generațiile trecute și viitoare, și cheia pentru înțelegerea și potențial tratarea multor boli care afectează umanitatea.
De la descoperirea structurii sale în dublă elice de către Watson și Crick până la proiectele de secvențiere a genomului uman și tehnicile moderne de editare genetică, ADN-ul continuă să fascineze și să inspire oamenii de știință și publicul larg deopotrivă.
Pe măsură ce tehnologiile de analiză și manipulare a ADN-ului continuă să evolueze, ne putem aștepta la progrese remarcabile în medicină, agricultură, biotehnologie și multe alte domenii. Aceste progrese vor aduce cu sine atât oportunități extraordinare, cât și provocări etice și sociale complexe pe care societatea va trebui să le abordeze cu înțelepciune și responsabilitate.
În esență, studiul ADN-ului nu reprezintă doar o explorare a fundamentelor biologice ale vieții, ci și o călătorie fascinantă de auto-descoperire a speciei umane, oferindu-ne perspective profunde despre cine suntem, de unde venim și încotro ne îndreptăm.