Ciclul Krebs
- Detalii
- Categorie: Biochimie
- Accesări: 1,356
Ciclul Krebs, cunoscut și sub denumirea de ciclul acidului citric sau ciclul acidului tricarboxilic (TCA), reprezintă una dintre cele mai fundamentale căi metabolice din corpul uman și al tuturor organismelor aerobe. Acest proces biochimic complex are loc în mitocondrii, "centralele energetice" ale celulelor, și joacă un rol esențial în producerea energiei necesare pentru toate funcțiile vitale ale organismului.
Descoperit în 1937 de către biochimistul german Hans Adolf Krebs, pentru care a primit Premiul Nobel pentru Medicină în 1953, ciclul Krebs reprezintă punctul central al metabolismului energetic celular. În acest articol, vom explora în detaliu mecanismele biochimice ale ciclului Krebs, importanța sa pentru sănătatea organismului, legăturile cu alte căi metabolice și implicațiile sale în diverse condiții medicale.
Ce este ciclul Krebs și unde are loc
Ciclul Krebs, sau ciclul acidului citric, este o serie de reacții biochimice care convertesc carbohidrații, grăsimile și proteinele în dioxid de carbon, apă și, cel mai important, energie sub formă de ATP (adenozin trifosfat) și coenzime reduse (NADH și FADH₂).
Acest proces vital are loc în matricea mitocondrială, spațiul intern al mitocondriilor. Mitocondriile sunt organite celulare prezente în majoritatea celulelor eucariote și sunt adesea numite "uzinele de energie" ale celulei datorită rolului lor crucial în producerea ATP-ului.
Localizarea precisă în celulă
Ciclul Krebs nu se întâmplă la întâmplare în celulă, ci într-un compartiment specific:
- Celulă eucariotă - Doar organismele cu celule eucariote (care conțin nucleu și organite membranare) posedă mitocondrii și, prin urmare, utilizează ciclul Krebs.
- Mitocondrie - Aceste organite au două membrane: una externă și una internă.
- Matricea mitocondrială - Spațiul înconjurat de membrana internă a mitocondriei, unde enzimele ciclului Krebs sunt localizate.
Această compartimentare specifică permite reglarea precisă a procesului și conexiunea eficientă cu alte căi metabolice.
Etapele ciclului Krebs
Ciclul Krebs este o secvență circulară de opt reacții biochimice. Pentru a înțelege întregul proces, vom analiza fiecare etapă în parte, evidențiind enzimele implicate, substraturile și produșii fiecărei reacții.
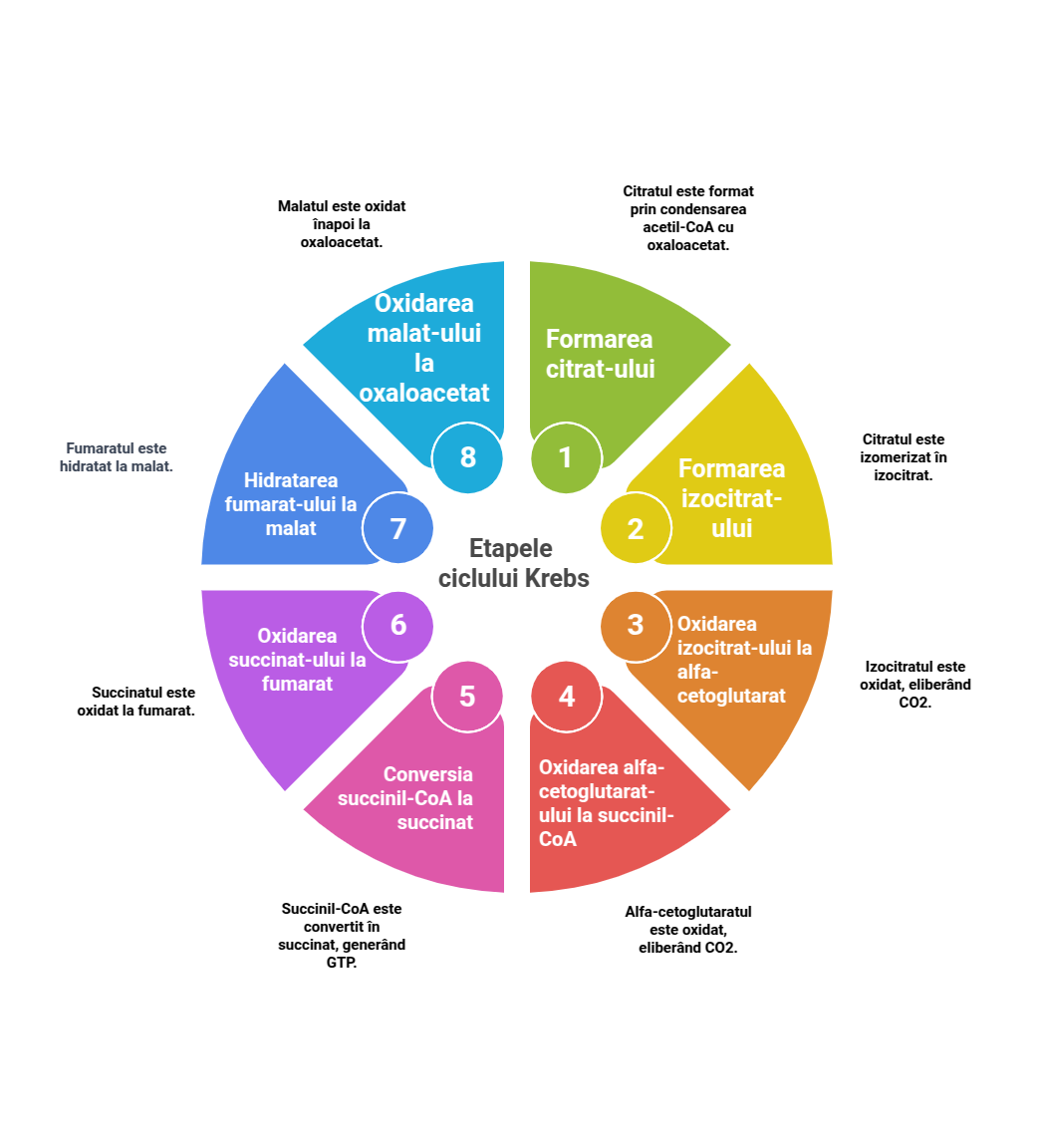
1. Formarea citrat-ului
Prima etapă a ciclului implică condensarea acetil-CoA cu oxaloacetatul pentru a forma citrat.
- Enzima: Citrat sintaza
- Substrat: Acetil-CoA și oxaloacetat
- Produs: Citrat și CoA (coenzima A)
Acetil-CoA, derivat din metabolismul carbohidraților (prin glicoliză și decarboxilarea oxidativă a piruvatului), al grăsimilor (prin beta-oxidare) sau al proteinelor (prin degradarea aminoacizilor), este principalul "combustibil" care intră în ciclul Krebs.
2. Formarea izocitrat-ului
În această etapă, citratul este rearanjat pentru a forma izocitratul.
- Enzima: Aconitaza
- Substrat: Citrat
- Intermediar: cis-Aconitat
- Produs: Izocitrat
Această reacție implică o deshidratare inițială, urmată de o rehidratare, rezultând o schimbare în poziția grupării hidroxil.
3. Oxidarea izocitrat-ului la alfa-cetoglutarat
Izocitratul este oxidat și decarboxilat, eliberând primul molecule de CO₂ din ciclu.
- Enzima: Izocitrat dehidrogenaza
- Substrat: Izocitrat și NAD⁺
- Produse: Alfa-cetoglutarat, NADH + H⁺ și CO₂
Această reacție reprezintă primul pas în care energia este captată sub formă de NADH.
4. Oxidarea alfa-cetoglutarat-ului la succinil-CoA
Alfa-cetoglutaratul suferă o decarboxilare oxidativă, eliberând a doua moleculă de CO₂.
- Enzima: Complexul alfa-cetoglutarat dehidrogenaza
- Substrat: Alfa-cetoglutarat, NAD⁺ și CoA
- Produse: Succinil-CoA, NADH + H⁺ și CO₂
Această reacție complexă implică cinci cofactori și generează o altă moleculă de NADH.
5. Conversia succinil-CoA la succinat
Succinil-CoA este transformat în succinat, cu generarea unei molecule de GTP (guanozin trifosfat) sau ATP.
- Enzima: Succinil-CoA sintetaza
- Substrat: Succinil-CoA, GDP și Pi (fosfat anorganic)
- Produse: Succinat, CoA și GTP
Aceasta este singura etapă din ciclul Krebs unde ATP (sau echivalentul său, GTP) este generat direct prin fosforilare la nivel de substrat.
6. Oxidarea succinat-ului la fumarat
Succinatul este oxidat la fumarat, cu generarea FADH₂.
- Enzima: Succinat dehidrogenaza
- Substrat: Succinat și FAD
- Produse: Fumarat și FADH₂
Această enzimă este unică deoarece este încorporată în membrana internă mitocondrială și face parte din complexul II al lanțului respirator.
7. Hidratarea fumarat-ului la malat
Fumaratul este hidratat pentru a forma L-malat.
- Enzima: Fumaraza
- Substrat: Fumarat și H₂O
- Produs: L-malat
8. Oxidarea malat-ului la oxaloacetat
În ultima etapă, malatul este oxidat pentru a regenera oxaloacetatul, care poate începe un nou ciclu.
- Enzima: Malat dehidrogenaza
- Substrat: L-malat și NAD⁺
- Produse: Oxaloacetat și NADH + H⁺
Cu regenerarea oxaloacetatului, ciclul este complet și pregătit să accepte o nouă moleculă de acetil-CoA.
Bilanțul energetic al ciclului Krebs
Pentru fiecare moleculă de acetil-CoA care intră în ciclul Krebs, bilanțul energetic este:
- 3 molecule de NADH (produse în etapele 3, 4 și 8)
- 1 moleculă de FADH₂ (produsă în etapa 6)
- 1 moleculă de GTP/ATP (produsă în etapa 5)
- 2 molecule de CO₂ eliberate (în etapele 3 și 4)
Coenzimele reduse (NADH și FADH₂) sunt ulterior utilizate în lanțul transportor de electroni (lanțul respirator) pentru a genera ATP prin fosforilare oxidativă. Fiecare NADH poate produce aproximativ 2,5 molecule de ATP, iar FADH₂ poate genera aproximativ 1,5 molecule de ATP.
Astfel, un singur ciclu Krebs poate duce la producerea teoretică de aproximativ 10 molecule de ATP prin fosforilare oxidativă, plus 1 GTP/ATP direct din ciclu:
- 3 NADH × 2,5 ATP = 7,5 ATP
- 1 FADH₂ × 1,5 ATP = 1,5 ATP
- 1 GTP/ATP = 1 ATP
- Total: aproximativ 10 ATP
Conexiuni cu alte căi metabolice
Ciclul Krebs nu funcționează izolat, ci este integrat perfect cu alte căi metabolice esențiale.
Legătura cu glicoliza
Glicoliza, procesul de descompunere a glucozei în două molecule de piruvat, are loc în citoplasmă. Piruvatul rezultat este transportat în mitocondrie, unde este convertit în acetil-CoA prin decarboxilare oxidativă, care apoi intră în ciclul Krebs.
Legătura cu oxidarea acizilor grași
Acizii grași sunt degradați prin beta-oxidare, generând multiple molecule de acetil-CoA, care alimentează ciclul Krebs. Această cale este deosebit de importantă în timpul postului sau exercițiului fizic prelungit, când rezervele de grăsime sunt mobilizate pentru energie.
Legătura cu metabolismul aminoacizilor
Aminoacizii proveniți din degradarea proteinelor pot fi convertiți în diferite intermediari ai ciclului Krebs. De exemplu:
- Aminoacizii cetogenici (leucină, lizină) sunt transformați în acetil-CoA
- Aminoacizii gluconeogenici (alanină, cisteină) sunt convertiți în piruvat
- Alți aminoacizi (glutamat, glutamină) pot fi convertiți în alfa-cetoglutarat
Legătura cu lanțul respirator
Coenzimele reduse (NADH și FADH₂) produse în ciclul Krebs transferă electronii lor către lanțul transportor de electroni din membrana internă mitocondrială. Acest proces generează un gradient electrochimic de protoni, care alimentează sinteza ATP prin ATP sintază (fosforilare oxidativă).
Legătura cu gluconeogeneza
În condiții de nivel scăzut de glucoză, anumite intermediare ale ciclului Krebs pot fi extrase și utilizate pentru sinteza de glucoză prin gluconeogeneză. Acest proces este esențial pentru menținerea glicemiei în timpul postului.
Reglarea ciclului Krebs
Fiind o cale metabolică centrală, ciclul Krebs este strâns reglat pentru a răspunde nevoilor energetice celulare și pentru a se adapta la diferite condiții metabolice.
Reglarea prin disponibilitatea substraturilor
Disponibilitatea acetil-CoA, oxaloacetatului și a cofactorilor (NAD⁺, FAD) influențează direct rata ciclului Krebs.
Reglarea alosterică
Enzimele ciclului Krebs sunt reglate alosteric de diverși metaboliți:
- Citrat sintaza este inhibată de ATP, NADH și succinil-CoA
- Izocitrat dehidrogenaza este activată de ADP și inhibată de ATP și NADH
- Complexul alfa-cetoglutarat dehidrogenaza este inhibat de succinil-CoA și NADH
Reglarea prin modificări covalente
Unele enzime din ciclul Krebs pot fi modificate prin fosforilare/defosforilare, afectându-le activitatea.
Reglarea hormonală
Hormonii precum insulina, glucagonul și adrenalina influențează indirect ciclul Krebs prin efectele lor asupra glicolizei, lipolizei și metabolismului proteic.
Importanța ciclului Krebs pentru sănătate
Funcționarea optimă a ciclului Krebs este esențială pentru sănătatea umană, având implicații în numeroase procese fiziologice și condiții patologice.
Producerea energiei
Rolul principal al ciclului Krebs este de a genera energie. Un ciclu Krebs eficient asigură producerea adecvată de ATP pentru toate procesele celulare energo-dependente.
Metabolismul nutrienților
Ciclul Krebs reprezintă punctul de convergență pentru metabolismul carbohidraților, lipidelor și proteinelor, permițând organismului să utilizeze eficient diverși nutrienți pentru energie.
Biosinteza
Pe lângă rolul său în catabolism, ciclul Krebs furnizează intermediari pentru diverse căi anabolice:
- Citrat pentru sinteza acizilor grași
- Alfa-cetoglutarat pentru sinteza aminoacizilor
- Succinil-CoA pentru sinteza hemului
Detoxifierea
Unele enzime asociate cu ciclul Krebs participă la detoxifierea xenobioticelor și metaboliților potențial dăunători.
Disfuncții și afecțiuni asociate cu ciclul Krebs
Perturbările în funcționarea ciclului Krebs pot duce la diverse afecțiuni și simptome clinice.
Boli mitocondriale
Mutațiile în genele care codifică enzimele ciclului Krebs sau proteinele implicate în funcționarea mitocondriilor pot duce la boli mitocondriale. Aceste afecțiuni rare sunt caracterizate prin producție insuficientă de energie și pot afecta multiple organe, în special cele cu cerințe energetice ridicate, precum creierul, mușchii și inima.
Exemple de boli mitocondriale includ:
- Sindromul Leigh
- Neuropatia optică ereditară Leber
- Sindromul MELAS (encefalomiopatie mitocondrială, acidoză lactică și episoade similare accidentului vascular cerebral)
Cancer
Mutațiile în genele care codifică anumite enzime ale ciclului Krebs au fost asociate cu dezvoltarea unor tipuri de cancer. De exemplu:
- Mutațiile în gena pentru fumarat hidratază sunt legate de carcinomul renal ereditar și leiomiomatoza
- Mutațiile în genele pentru succinat dehidrogenază au fost asociate cu feocromocitomul și paragangliomul
În plus, multe celule canceroase prezintă un metabolism energetic alterat, cunoscut sub numele de efectul Warburg, caracterizat prin dependența crescută de glicoliză aerobă în loc de ciclul Krebs și fosforilare oxidativă.
Boli neurodegenerative
Disfuncția mitocondrială și perturbarea ciclului Krebs au fost implicate în patogeneza mai multor boli neurodegenerative, inclusiv:
- Boala Alzheimer
- Boala Parkinson
- Scleroza laterală amiotrofică (SLA)
- Boala Huntington
Diabetul și rezistența la insulină
Perturbările în funcționarea ciclului Krebs pot contribui la dezvoltarea rezistenței la insulină și a diabetului de tip 2. Acumularea excesivă de intermediari ai ciclului Krebs a fost asociată cu disfuncția mitocondrială și stresul oxidativ în celulele pancretice și mușchii scheletici.
Obezitatea și sindromul metabolic
Disfuncțiile în ciclul Krebs și metabolismul mitocondrial au fost implicate în dezvoltarea obezității și a sindromului metabolic. Eficiența redusă a ciclului Krebs poate duce la o capacitate diminuată de oxidare a acizilor grași și la acumularea lipidelor.
Strategii pentru optimizarea funcționării ciclului Krebs
Există mai multe abordări care pot ajuta la menținerea sau îmbunătățirea funcționării ciclului Krebs.
Nutriție adecvată
O alimentație echilibrată, bogată în nutrienți, asigură toate substraturile și cofactorii necesari pentru ciclul Krebs:
- Vitaminele B (B1, B2, B3, B5) sunt esențiale pentru multe enzime ale ciclului Krebs
- Minerale precum magneziu, mangan și fier sunt necesare pentru funcționarea optimă a enzimelor
- Antioxidanții protejează mitocondriile de stresul oxidativ
Exercițiu fizic regulat
Activitatea fizică stimulează biogeneza mitocondrială și îmbunătățește eficiența ciclului Krebs. Exercițiile aerobice sunt deosebit de benefice pentru metabolismul mitocondrial.
Gestionarea stresului
Stresul cronic poate afecta negativ funcționarea mitocondriilor și ciclul Krebs. Tehnicile de relaxare, meditația și un somn adecvat pot ajuta la reducerea stresului oxidativ și la îmbunătățirea metabolismului energetic.
Suplimente potențial benefice
Anumite suplimente pot sprijini funcționarea ciclului Krebs:
- Coenzima Q10
- L-carnitină
- Acid alfa-lipoic
- Acid succinic
- Resveratrol
Este important de menționat că eficacitatea acestor suplimente variază și este recomandată consultarea unui specialist înainte de utilizare.
Cercetări recente și perspective de viitor
Cercetările asupra ciclului Krebs continuă să evolueze, oferind noi perspective asupra rolului său în sănătate și boală.
Rolul în inflamație și imunitate
Studii recente au evidențiat legăturile dintre metabolismul energetic și răspunsul imun. Intermediarii ciclului Krebs, precum succinatul și fumaratul, au fost identificați ca molecule de semnalizare care influențează activarea celulelor imune și răspunsul inflamator.
Terapii mitocondriale țintite
Dezvoltarea de terapii care vizează specific mitocondriile și ciclul Krebs reprezintă o direcție promițătoare în tratamentul bolilor mitocondriale, neurodegenerative și metabolice.
Ciclul Krebs în medicina de precizie
Profilurile metabolice individuale, inclusiv funcționarea ciclului Krebs, ar putea fi utilizate pentru personalizarea intervențiilor medicale și nutriționale.
Ciclul Krebs și longevitatea
Optimizarea funcționării ciclului Krebs și a metabolismului mitocondrial este investigată ca o potențială strategie pentru încetinirea îmbătrânirii și prelungirea vieții sănătoase.
Concluzii
Ciclul Krebs reprezintă o cale metabolică fundamentală care stă la baza producerii de energie în organismele aerobe. Importanța sa depășește cu mult funcția de generare a ATP, având implicații în numeroase procese biologice, de la biosinteza macromoleculelor până la reglarea răspunsului imun.
Înțelegerea aprofundată a ciclului Krebs și a interconexiunilor sale cu alte căi metabolice oferă perspective valoroase asupra funcționării normale a organismului și a mecanismelor implicate în diverse afecțiuni. Pe măsură ce cercetarea științifică avansează, cunoștințele despre ciclul Krebs continuă să se îmbogățească, deschizând noi posibilități pentru intervenții terapeutice și strategii preventive.
În era medicinei personalizate și a intervențiilor nutriționale țintite, optimizarea funcționării ciclului Krebs ar putea reprezenta o abordare promițătoare pentru îmbunătățirea sănătății metabolice, prevenirea bolilor cronice și promovarea longevității.
Întrebări frecvente despre ciclul Krebs
1. Ce este ciclul Krebs și de ce este important pentru organismul uman?
Răspuns: Ciclul Krebs (sau ciclul acidului citric) reprezintă o serie de reacții biochimice care au loc în mitocondrii și care transformă acetil-CoA în energie sub formă de ATP și coenzime reduse (NADH și FADH₂). Importanța sa este fundamentală deoarece reprezintă punctul central al metabolismului energetic celular, fiind calea comună finală pentru oxidarea carbohidraților, proteinelor și lipidelor. Fără funcționarea corectă a ciclului Krebs, celulele nu ar putea produce suficientă energie pentru a susține procesele vitale, ceea ce ar duce la disfuncții celulare grave și, în cele din urmă, la moarte celulară.
2. Cum este conectat ciclul Krebs cu alte căi metabolice din organism?
Răspuns: Ciclul Krebs funcționează ca un nod central în metabolismul celular, fiind conectat cu multiple căi metabolice:
- Cu glicoliza: Piruvatul rezultat din glicoliză este transformat în acetil-CoA, care intră în ciclul Krebs.
- Cu oxidarea acizilor grași: Beta-oxidarea acizilor grași generează acetil-CoA, care alimentează ciclul.
- Cu metabolismul aminoacizilor: Aminoacizii pot fi convertiți în diferiți intermediari ai ciclului Krebs (ex: glutamatul în alfa-cetoglutarat).
- Cu lanțul respirator: NADH și FADH₂ produse în ciclul Krebs transferă electronii către lanțul transportor de electroni pentru generarea ATP.
- Cu gluconeogeneza: Intermediarii ciclului Krebs pot fi extrași și utilizați pentru sinteza de glucoză.
- Cu diverse căi biosintetice: Intermediarii ciclului furnizează substrat pentru sinteza acizilor grași, aminoacizilor și altor biomolecule.
3. Care sunt principalele disfuncții asociate cu ciclul Krebs și cum se manifestă acestea?
Răspuns: Disfuncțiile ciclului Krebs pot duce la diverse afecțiuni:
- Boli mitocondriale: Cauzate de mutații în genele ce codifică enzimele ciclului sau proteinele implicate în funcționarea mitocondriilor. Acestea se manifestă prin simptome precum slăbiciune musculară, intoleranță la efort, probleme neurologice și cardiace.
- Cancer: Mutații în genele pentru fumarat hidratază sau succinat dehidrogenază sunt asociate cu anumite tipuri de cancer (carcinom renal, feocromocitom). Multe celule canceroase prezintă efectul Warburg, cu dependență crescută de glicoliză în detrimentul ciclului Krebs.
- Boli neurodegenerative: Disfuncția mitocondrială și perturbarea ciclului Krebs contribuie la patogeneza bolilor Alzheimer, Parkinson, SLA și Huntington.
- Diabet și rezistență la insulină: Perturbările în ciclul Krebs pot contribui la disfuncția celulelor beta pancreatice și la rezistența la insulină.
- Obezitate și sindrom metabolic: Eficiența redusă a ciclului Krebs duce la capacitate diminuată de oxidare a acizilor grași și acumulare de lipide.
4. Cum poate fi optimizată funcționarea ciclului Krebs prin intervenții dietetice și stil de viață?
Răspuns: Funcționarea ciclului Krebs poate fi optimizată prin:
- Nutriție adecvată: Consumul de alimente bogate în vitamine B (carne, ouă, leguminoase, cereale integrale), minerale (magneziu, fier, mangan) și antioxidanți (fructe și legume colorate).
- Exercițiu fizic regulat: Activitatea fizică, în special de tip aerobic, stimulează biogeneza mitocondrială și îmbunătățește eficiența ciclului Krebs.
- Gestionarea stresului: Tehnici de relaxare, meditație și somn adecvat reduc stresul oxidativ și îmbunătățesc metabolismul energetic.
- Perioadele de post intermitent: Pot stimula funcționarea mitocondrială și activează căi metabolice alternative.
- Expunerea la frig controlat: Poate stimula biogeneza mitocondrială și metabolismul energetic.
- Suplimente specifice: (sub supraveghere medicală) CoQ10, L-carnitină, acid alfa-lipoic, acid succinic, resveratrol pot sprijini funcționarea ciclului Krebs.
5. Care este bilanțul energetic al ciclului Krebs și cum contribuie la producția totală de ATP a celulei?
Răspuns: Pentru fiecare moleculă de acetil-CoA care intră în ciclul Krebs, bilanțul energetic este:
- 3 molecule de NADH (generate în etapele 3, 4 și 8)
- 1 moleculă de FADH₂ (generată în etapa 6)
- 1 moleculă de GTP/ATP (generată direct în etapa 5)
- 2 molecule de CO₂ eliberate
În lanțul respirator, fiecare NADH poate genera aproximativ 2,5 molecule de ATP, iar FADH₂ aproximativ 1,5 molecule ATP. Astfel, un singur ciclu complet poate duce la producerea teoretică de aproximativ 10 molecule de ATP:
- 3 NADH × 2,5 ATP = 7,5 ATP
- 1 FADH₂ × 1,5 ATP = 1,5 ATP
- 1 GTP/ATP = 1 ATP
Deși ciclul Krebs în sine contribuie direct cu doar o moleculă de GTP/ATP, rolul său în generarea coenzimelor reduse care alimentează lanțul respirator îl face esențial pentru producția eficientă de energie celulară. Pentru comparație, glicoliza anaerobă produce doar 2 molecule de ATP pe moleculă de glucoză, în timp ce oxidarea completă a glucozei prin glicoliză, ciclul Krebs și fosforilare oxidativă poate genera până la 30-32 molecule de ATP.
Referințe și resurse suplimentare
Pentru o înțelegere mai aprofundată a ciclului Krebs, consultați următoarele resurse:
- Krebs, H. A., & Johnson, W. A. (1937). The role of citric acid in intermediate metabolism in animal tissues. Enzymologia, 4, 148-156.
- Berg, J. M., Tymoczko, J. L., & Stryer, L. (2012). Biochemistry (7th ed.). W. H. Freeman and Company.
- Nelson, D. L., & Cox, M. M. (2017). Lehninger Principles of Biochemistry (7th ed.). W. H. Freeman and Company.
- Alberts, B., Johnson, A., Lewis, J., Morgan, D., Raff, M., Roberts, K., & Walter, P. (2014). Molecular Biology of the Cell (6th ed.). Garland Science.
- Wallace, D. C. (2012). Mitochondria and cancer. Nature Reviews Cancer, 12(10), 685-698.
- Spinelli, J. B., & Haigis, M. C. (2018). The multifaceted contributions of mitochondria to cellular metabolism. Nature Cell Biology, 20(7), 745-754.
- Mills, E. L., Kelly, B., & O'Neill, L. A. J. (2017). Mitochondria are the powerhouses of immunity. Nature Immunology, 18(5), 488-498.
- Shadel, G. S., & Horvath, T. L. (2015). Mitochondrial ROS signaling in organismal homeostasis. Cell, 163(3), 560-569.
- Ryan, D. G., Murphy, M. P., Frezza, C., Prag, H. A., Chouchani, E. T., O'Neill, L. A., & Mills, E. L. (2019). Coupling Krebs cycle metabolites to signalling in immunity and cancer. Nature Metabolism, 1(1), 16-33.
- López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M., & Kroemer, G. (2013). The hallmarks of aging. Cell, 153(6), 1194-1217.